全球医药健康产业政策举措出现了哪些新特征?
作者:苏州市医药产品公平贸易工作站来源:中国医药保健品进出口商会 点击数: 84发布时间:2022年4月11日
近年来,围绕生物技术制高点占据,以及医药健康产业发展新动力的培育,各国相继发布了加快医疗生物技术创新突破的政策举措。同时,欧美各国持续加强同中国生物科技战略竞争,重视本国医疗健康领域的供应链保障。在医药健康产业全球化融合发展的趋势下,各国持续加强监管合作,以保障药品供应,促进产业创新发展。
01 世界主要经济体推动医疗生物技术创新突破
美国创新组织模式,探索成立国家级研究平台,强化国家战略科技力量,破解医学研究创新的运行机制瓶颈
美国拜登政府于2021年4月提议,拟成立“高级健康研究计划局” (ARPA-H)。该部门依托美国国立卫生研究院(NIH)运作,申请预算为65亿美元,以美国国防部高级研究计划局(DARPA)为模型,通过资助高风险的创新项目来加快医疗技术的发展,尤其关注癌症、糖尿病和阿尔茨海默病的防治,同时追求其他能够重塑健康研究的“变革性创新”。从现有的资助机制看,NIH对科学项目的支持倾向于渐进的、假设驱动的研究,商业化部门则要求在合理的时限内获得预期的投资回报,以吸引投资者,一些最具潜力的创新想法可能因此而永远无法成熟。尽管ARPA-H的建立仍有争议,但其从组织模式、项目资助机制方面进行探索,为创新想法提供理想的平台,对医学和健康领域的突破性技术和广泛适用的平台、资源和解决方案进行关键投资,造福所有患者。这些投资活动通常无法通过传统基础研究和商业活动来轻易实现。
美国科技智库信息技术与创新基金会于2021年6月发布《确保美国生物制药持续竞争力》报告,建议为确保美国生物制药领域全球领导地位,应制定强有力的国家生物制药竞争力战略,更多投资于注重生物医学创新的产业-大学伙伴关系,NIH应增加至少120亿美元资助基金,达到每年500亿美元。
多国出台新的战略规划,持续修订推进和完善中长期战略部署
日本于2019年6月出台《集成创新战略2019》,并在附件中正式推出《生物战略2019》,这是继《生物技术战略大纲》(2002年)、《促进生物技术创新根本性强化措施》(2008年)战略之后,再次确认了生物技术的战略地位。此次战略将“医疗与非医疗领域”整合在一起进行通盘考虑,重点发展高性能生物材料、生物塑料、生物药物、生物制造系统等领域,并进行重点资助。同时在生物资源库、生物数据科技设施、生物科技人才等方面也提出重要举措。
俄罗斯发布《2019-2027年俄罗斯联邦基因技术发展规划》,该规划的主要目标是加速发展基因编辑技术等基因技术,为医学、农业和工业创造科技储备,并监测和预防生物性紧急情况的发生。韩国发布《生物健康产业创新战略》,以推进创新药、医疗器械和医疗技术发展,推动生物健康产业出口增长。英国发布《生物科技领域实施计划2019》,以发展前沿生物科技、应对战略挑战并夯实技术发展基础。法国2021年发布《法国医药卫生创新2030战略》,重点宣布创建大型科研“集群”,拟动用逾40亿欧元的公共资金用于科研,旨在重新将法国塑造成一个医药卫生领域的创新国家。
02 更加重视本国供应链保障
在新冠肺炎疫情爆发后,世界各国对生物医药的需求愈发扩大,都出现了药品及医疗物资短缺的问题,各政府都积极采取措施保障供应链稳定。
欧盟计划更新立法,加强政策激励和惩戒措施,保障药品供应
在新冠肺炎疫情初期,欧盟在从中国和印度获取药品和药物成分方面遇到了困难,欧委会估计供应全球的原料药有三分之二在印度和中国生产。
为解决由于生产商过少、供应链脆弱、财政激励措施不足等原因造成的药品短缺问题,欧盟正考虑制定更严格的药品供应规定,以确保药品供应。2020年11月份发布《欧洲药物战略》,在战略的四大支柱中包括了增强危机防范和应对机制,保障供应链的多样化和安全,解决药品短缺问题,针对这一项欧盟委员会寻求在制药商和监管机构之间进行更多对话,以提出旨在解决全球供应链中脆弱性的提案。欧盟计划从研发奖励、企业罚款等层面,要求制药企业制定应急计划,接受更严格的供应义务。欧盟卫生专员 Stella Kyriakides 在斯洛文尼亚举行的卫生部长会议上表示,“我们需要更新立法,以弥补在统一报告、供应义务和供应链透明度等方面的不足。”欧委会计划于2022年12月提出立法提案。
美国计划提高国内API制造能力
由FDA和ASPR牵头的白宫报告指出,美国的药品供应链越来越依赖国外制造的药品、活性药物成分(API)以及关键起始材料。同时报告建议促进美国本地的生产工作以及国际合作,推动创新型制造工艺的建立和生产技术的研究与开发。
美国白宫、美国卫生与公众服务部(HHS)、美国食品药品监督管理局(FDA)于2021年6月份发布了旨在确保美国药品供应链安全的政策建议,HHS初步承诺提供近6000万美元,用于开发旨在提高国内API制造能力的新型平台技术,以减少对全球药品供应链的依赖。
各国支持原料药生产迁回本土
新冠疫情凸显“原料为王”的重要性,许多国家计划通过将原料药生产迁回本土,实现在本国恢复完整的产业链,以摆脱对其他国家原料药的进口依赖。
美欧日印等国家均宣布要实现关键药物和医疗产品的本土生产。如法国赛诺菲将其在欧洲的六个原料药(API)生产基地合并,创建一家独立的API生产公司,以平衡欧洲对亚洲原料药的依赖程度;日本为抵抗抗生素等品类缺货对医疗造成的巨大影响,盐野义制药最早将在2022年在岩手县启动手术用抗生素原料的生产;印度联邦内阁批准了一项13亿美元的刺激计划,重点扶持53种原料药及关键中间体的生产,出资在印度国内设立3个原料药园区。
03 欧美国家压制中国在生物科技领域的赶超
美国为保持其技术、科学等方面的领先地位,系统加强在生物科技领域的扶持和保护,持续强化对华生物技术的压制
美国正在以立法形式全面升级与中国前沿科技层面的竞争。2021年6月,美国参议院通过了《2021美国创新与竞争法案》,通过立法形式开启系统性制华时代,《2021年迎接中国挑战法案》是六部分内容之一。该法案将“生物技术、医疗技术、基因组学和合成生物学”被列为十大关键技术重点领域之一,并提出重点保护生物医学研究领域,特别是人类基因信息。
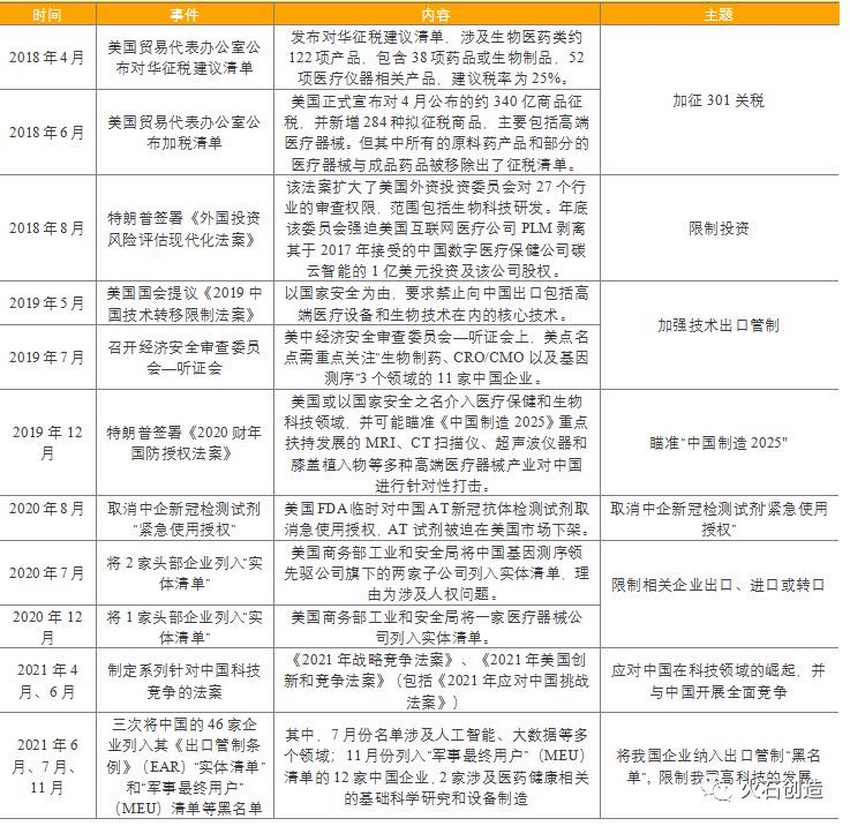
三年来,美国先后从层面加强对中国的打压,保持其在生物技术领域的领先地位。限制中国在美生物科技研发投资、对三百多项生物医药领域产品加征关税、禁止向中国出口生物技术、将生物技术头部企业列入“实体清单”、取消中企新冠检测试剂“紧急使用授权”等。
表1:美国对中国生物医疗领域的打压
欧盟也在防范中国在生物科技等特殊领域对欧投资
欧盟委员会在2020年3月发布了保护欧洲重要资产和技术的指导纲要,将健康、医学研究、生物技术等战略性产业纳入外资审查范围。6月,欧盟委员会发布防范不公平竞争政策白皮书,就加强监管欧盟外第三国政府补贴企业行为公开征求意见,进一步提高中国企业对欧投资门槛。同时,美国通过与欧盟等国家和组织在原有同盟基础上建立更加多样化的联盟关系,借助彼此的优势,联合遏制中国的发展,阻止中国超越美国,2021年12月,美常务副国务卿舍曼、欧盟对外行动署秘书长桑尼诺在华盛顿主持“美欧涉华对话”第二次会议并发表声明称,要实现供应链多元化,以解决中国经济胁迫。
04 监管与审批合作推动产业创新发展
生物医药基础研究、产品开发、市场流通和收并购仍将在全球更大范围内开展,药品的供应链保障、研发和监管专业知识方面都离不开多方的合作。主流国家的监管制度将出现趋同,特别是在涉及临床试验、现场核查和药物警戒等领域的规范会有更多融合,信息共享和交流互通愈加普遍。
美国与欧盟药品监管部门加强促进产品开发方面的信息共享,FDA 和 EMA 启动复杂仿制药-混合产品并行科学建议试点计划
美国 FDA 和欧洲药品管理局(EMA)于2021年9月宣布启动一项试点计划,为 FDA 复杂仿制药产品的简化新药申请(ANDA)和 EMA 混合产品上市许可申请(MAA)的申请人提供并行科学建议(PSA),该试点项目是 FDA 和 EMA 现有新药和生物制品 PSA 的扩展。PSA 试点计划的目标是为 FDA 和 EMA 审评人员提供一种机制,优化申请人的全球产品开发计划,以便在复杂仿制药/混合产品的开发阶段与申请人同时就科学问题交换意见,让申请人更深入地了解两家机构的监管决策基础,帮助申请人避免不必要的研究重复或不必要的多样化检测方法,缩短审批时间。
美欧加英等地区加强制药领域的反垄断合作,保障药品供应和促进创新
2021年3月,针对日益增加的制药领域的并购交易,欧盟委员会表示已经建立了专门的工作小组,将与美国、英国同行合作并分享有关如何审查制药行业并购的专业知识,对兼并交易进行更严格的审查,防止并购交易推高药物价格并阻碍创新。该工作小组将总结近年来并购方面的经验教训,探索并促进行业的竞争和创新。
近年来,欧美反垄断监管机构已逐渐加强对制药业并购以及可能危害消费者和竞争的其它做法进行审查,在反向支付协议、药品生命期专利策略等方面,通常是其关注的焦点问题。
国际中国加强药品监管国际化进程,与多国开展合作
我国监管国际化进程逐步加快,国家药监局先后与多个区域药品监管部门签署合作谅解备忘录,同时推动药品监管的国际交流活动开展,深化在药品、医疗器械和化妆品监管领域的合作。
2021年9月,由国家药监局和商务部共同主办的“一带一路”国家药品监管与发展合作研讨会暨“一带一路”国家医药监管合作与产业发展研修班开班仪式以线上线下相结合的方式在京举办,17个国家的卫生和药品监管机构相关官员和专家参加了研讨会。
2021年9月,由国家药监局和广西壮族自治区人民政府共同主办的第6届中国—东盟药品合作发展高峰论坛在广西防城港开幕。本届论坛以“强化药品医疗器械监管,共创产业精工智造发展”为主题,各国代表就药品监管法制建设、深化审评审批制度改革、抗击新冠肺炎疫情等方面展开深入交流和探讨。
2021年6月,中英药品监管合作项目启动会以视频形式召开,通过了2021年度中英药品监管合作项目计划,拟在药品审评、检查及上市后监测等领域开展技术交流活动,进一步增进了解,深化合作。中英两国药品监管机构曾于2018年1月签署《药品和医疗器械合作谅解备忘录》。
2021年4月,中国国家药品监督管理局与日本药品监管机构举行双边会议,就中日双边监管合作进行深入交流。中日两国监管机构曾在“2020中日医药健康交流会”上围绕《药品管理法》修订、临床试验管理、真实世界数据应用、药品上市后监管等热点问题展开主题报告并进行热烈讨论。
受新冠肺炎疫情影响,各国将更加重视公共卫生领域的科技发展,生命健康领域将成为全球科技创新的关键核心领域,各国将进一步加强相关基础研究,提升医疗健康关键核心技术攻关能力,增加疫病防控和公共卫生的战略科技力量储备,生命健康科技的科技战略竞争将进一步加剧,但同时各国将进一步加强监管合作,服务应对医药健康产业的全球化合作。 (火石创造)
